Die Versorgung von heute mit den Möglichkeiten von morgen verbinden
Die Versorgung von heute mit den Möglichkeiten von morgen verbinden

Autoimmunbedingte Interstitielle Lungenerkrankungen besser verstehen
ILD ist eine häufige, oft frühe und potenziell tödliche Manifestation autoimmuner Erkrankungen.1,2
Systemisch rheumatische Autoimmunerkrankungen (SARD) können zahlreiche Organe betreffen; besonders häufig ist jedoch die Lunge betroffen, meist in Form einer interstitiellen Lungenerkrankung (SARD-ILD).1-3
Autoimmunerkrankungen können Multiorganschäden verursachen; die Lunge ist jedoch besonders gefährdet und manifestiert sich häufig als ILD.3

SARD-ILD verstehen
Patient:innen mit SARD-ILD haben ein Risiko, eine Lungenfibrose zu entwickeln7,8
Duale Pathologie von autoimmunbedingten ILDs: entzündliche und fibrotische Veränderungen in der Lunge
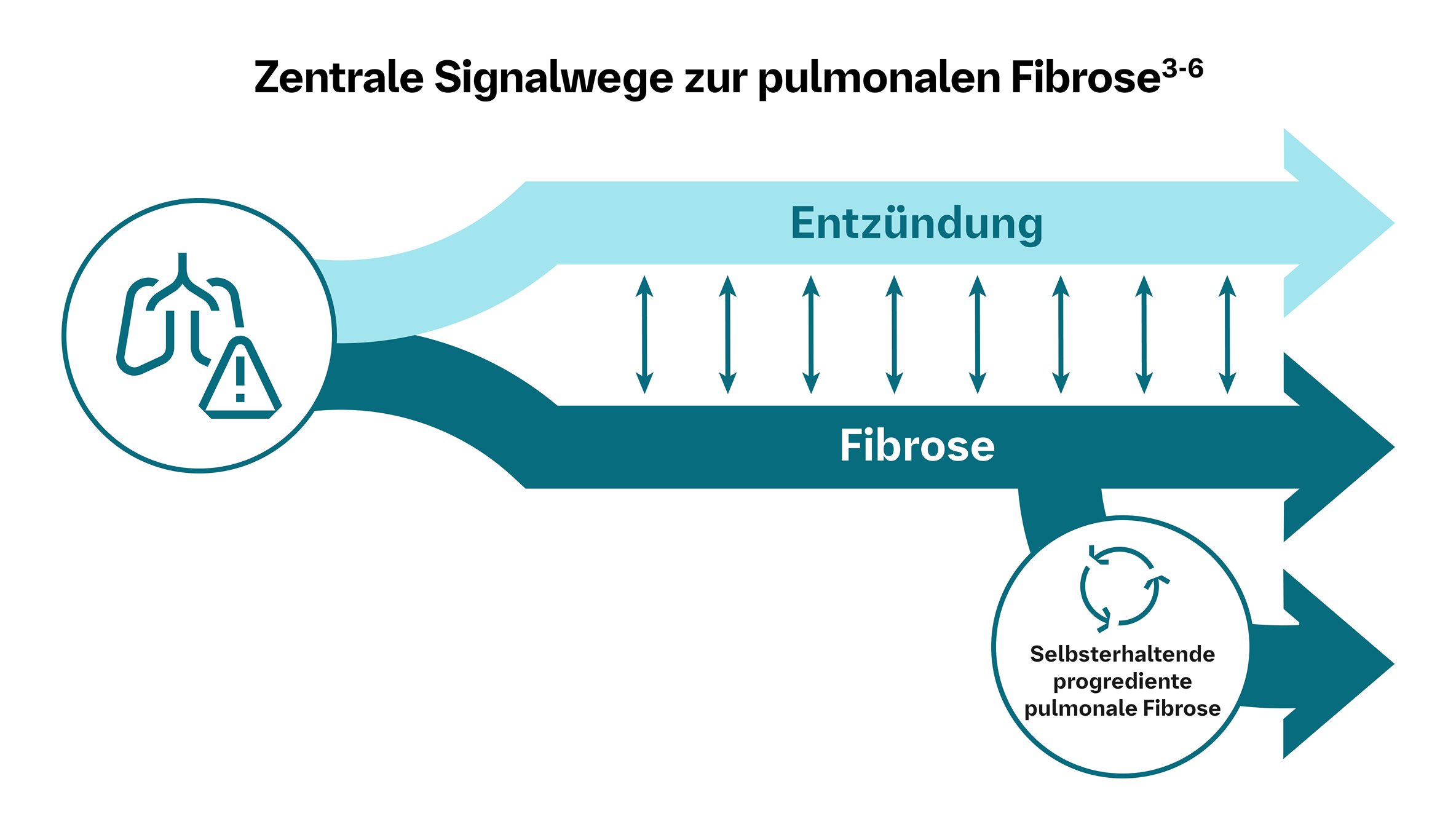
Patient:innen mit SARD-ILD sind häufig asymptomatisch oder berichten über unspezifische Symptome, was die Diagnosestellung erschweren kann15
Patient:innen können ein breites Spektrum an Symptomen zeigen, darunter:




Zahlreiche Erkrankungen mit vergleichbaren klinischen Zeichen und Symptomen erschweren die Differenzialdiagnostik zusätzlich.18
Progression verstehen
IPF und PPF sind lebensbedrohliche Erkrankungen.11
PPF – eine Gefahr für Ihre Patient:innen mit autoimmun-bedingten ILDs7,8
Progrediente Lungenfibrose (PPF) definiert als fortschreitende Lungenfibrose mit raschem Verlust der Lungenfunktion7,8
Bis zu 45 % der Patient:innen mit SARD-ILD können eine PPF entwickeln19
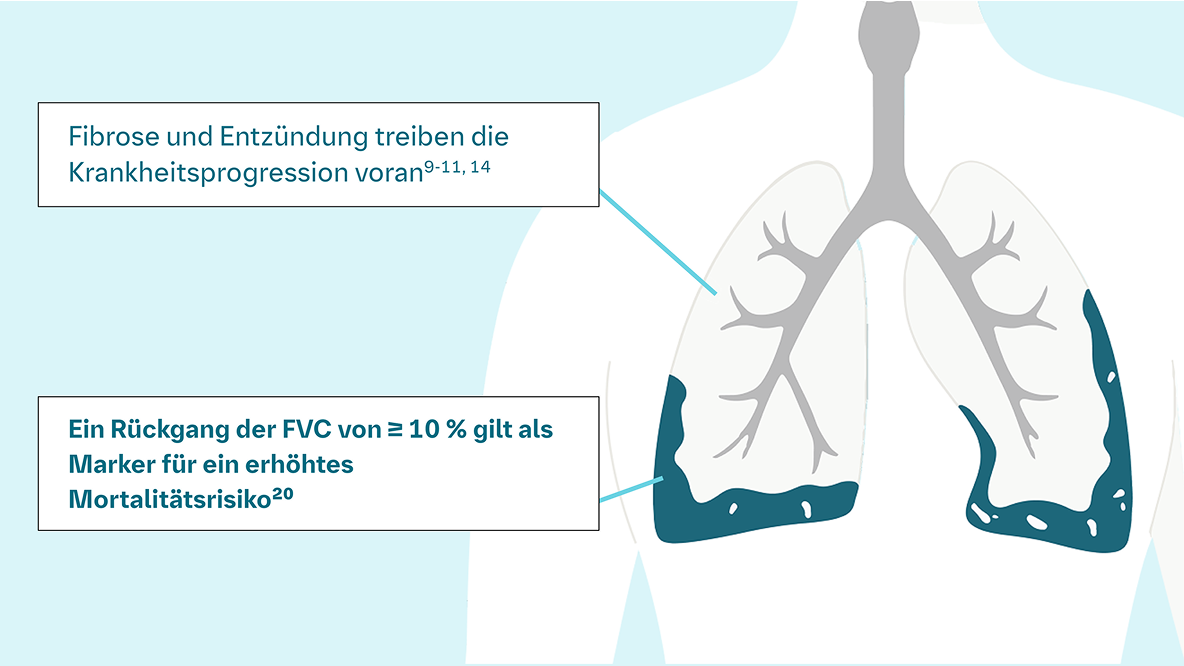
Bis zu 45 % der Patient:innen mit AI-ILD können eine PPF entwickeln19
PPF verlauft häufig tödlich9

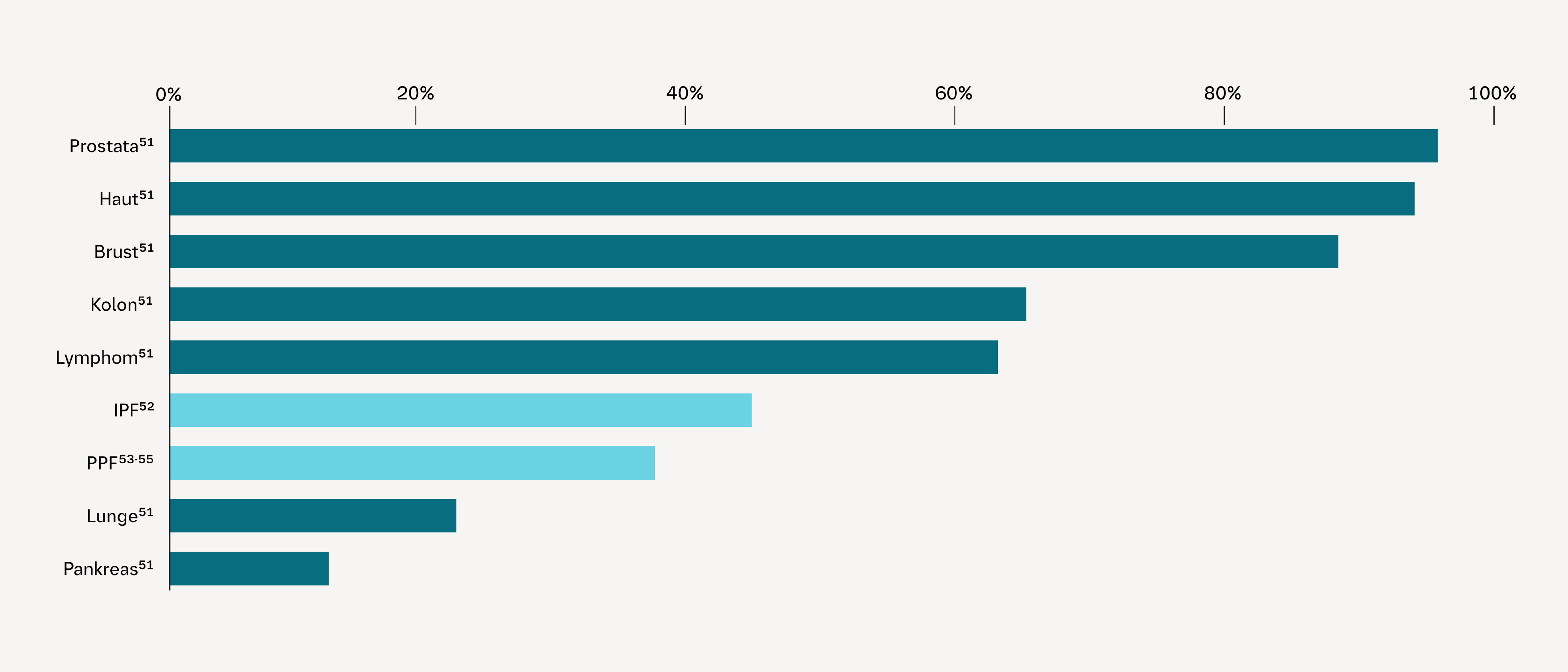
Die pulmonale Fibrose ist tödlicher als viele Krebsarten
5-Jahres-Überlebensraten*
Progression bei SARD-ILD frühzeitig erkennen – proaktives Monitoring ist entscheidend15

Aktuelle Behandlungsoptionen sind limitiert8,34
Trotz therapeutischer Fortschritte kommt es bei Patient:innen mit PPF weiterhin zu irreversiblen Lungenschäden und einer eingeschränkten Lebensqualität.8,34
Aktuelle Behandlungsansätze bei PPF:

Nintedanib ist die einzige zugelassene AF-Therapie zur Behandlung der PPF35,36

Geeignet für Patient:innen mit einer Sauerstoffsättigung unter 88 %37

Geeignet für Patient:innen mit hohem Sterberisiko und hoher Überlebenswahrscheinlichkeit8
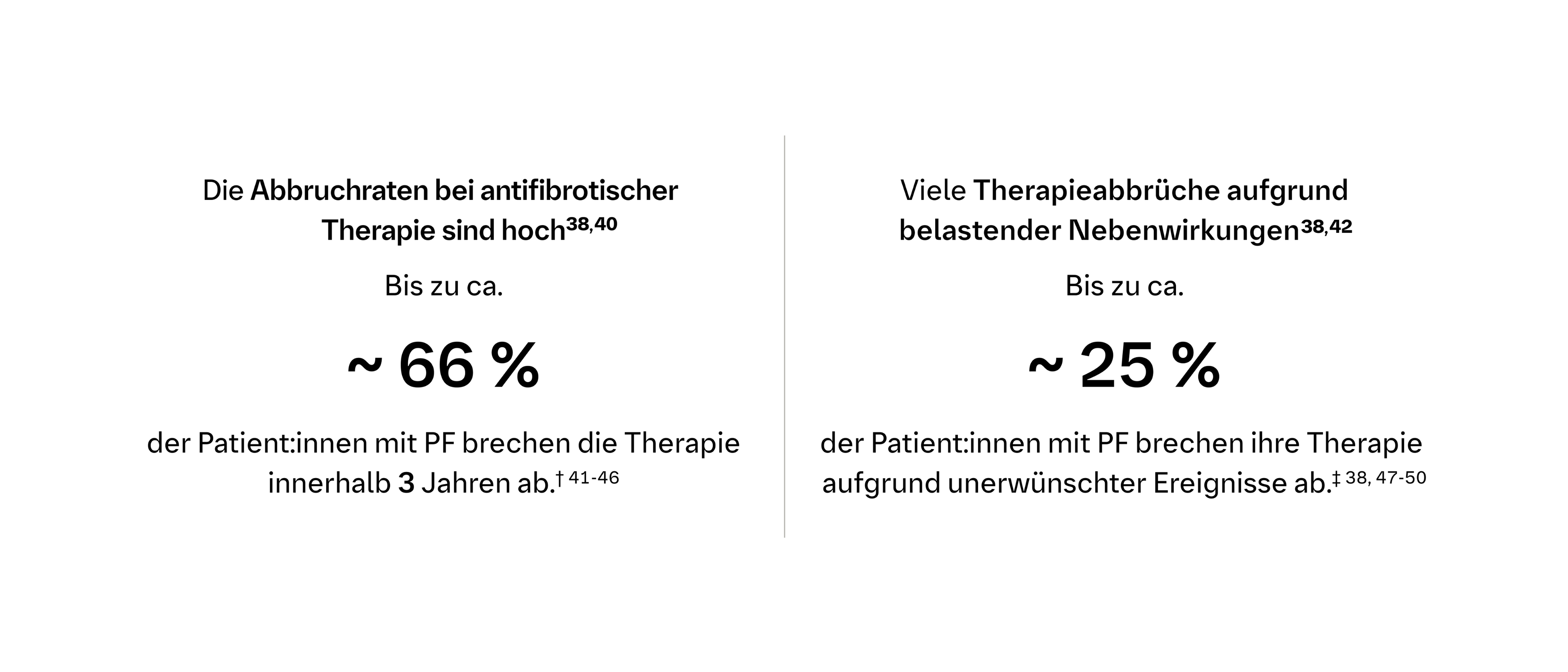
Einschränkungen aktueller Behandlungsoptionen können die Therapietreue beeinträchtigen38-40
Fußnoten:
ILD: interstitielle Lungenerkrankung; IPF: idiopathische pulmonale Fibrose; PPF: progrediente pulmonale Fibrose; HRCT: hochauflösende Computertomographie; DLCO: Diffusionskapazität der Lunge für Kohlenmonoxid; ALAT: Asociación Latinoamericana de Tórax; ATS: American Thoracic Society; ERS: European Respiratory Society; EULAR: European Alliance of Associations for Rheumatology; JRS: Japanese Respiratory Society; PF, pulmonale Fibrose.
*Grafik neu erstellt auf Grundlage von Daten aus Vancheri C. et al. (2010), Zheng Q. et al. (2022), Chen X. et al. (2021), Cen Z. et al. (2024) und Kwon BS. et al. (2021).
†Die Daten stammen aus sechs Publikationen: einer retrospektiven Studie mit Daten aus zwei Datenbanken aus den Zeiträumen Oktober 2013 bis März 2019 sowie Oktober 2014 bis September 2019 (n = 8 682 Patient:innen mit IPF);10 einer prospektiven Beobachtungsstudie aus den Jahren 2015 bis 2021 (n = 232 Patient:innen mit IPF);11 einer retrospektiven Beobachtungsstudie aus dem Zeitraum Oktober 2014 bis Juni 2018 (n = 1 455 Patient:innen mit IPF);12 einer multizentrischen retrospektiven Studie aus dem Zeitraum Januar 2013 bis April 2019 (n = 144 Patient:innen mit IPF);13 einer retrospektiven Studie aus dem Zeitraum Januar 2009 bis Dezember 2018 (n = 261 Patient:innen mit IPF);14 sowie einer retrospektiven Studie aus dem Zeitraum Februar 2017 bis Februar 2022 (n = 303 Patient:innen mit IPF).15
‡Die Daten stammen aus fünf Publikationen: einer narrativen Übersichtsarbeit zu Patient:innen und mit IPF;10 einer retrospektiven Studie aus dem Zeitraum September 2014 bis Februar 2016 (n = 186 Patient:innen mit PF);16 zwei randomisierten, doppelblinden Phase-III-Studien aus dem Zeitraum Mai 2011 bis September 2012 mit Patient:innen mit IPF (n = 1 066),17 einer randomisierten, doppelblinden Phase-III-Studie aus dem Zeitraum Februar 2017 bis April 2018 mit Patient:innen mit PPF (n = 663);18 sowie einer randomisierten Phase-III-Studie aus dem Zeitraum Juli 2011 bis Januar 2013 mit Patient:innen mit IPF (n = 555).19
Referenzen:
-
Wells AU, Denton CP. Nat Rev Rheumatol. 2014;10(12):728-739.
-
Wallace B, et al. Curr Opin Rheumatol. 2016;28(3):236-245.
-
Connerton Á, et al. Breathe (Sheff). 2025;21(2):240166.
-
Podolanczuk AJ, et al. Am J Respir Crit Care Med. 2025;211(7):1132-1155.
-
Joy GM, et al. Eur Respir Rev. 2023;32(167):220210.
-
Fischer A, et al. Eur Respir J. 2015;46(4):976-987.
-
Raghu G, et al. Am J Respir Crit Care Med. 2022;205(9):e18-e47.
-
Wijsenbeek M, Cottin V. N Engl J Med. 2020;383(10):958-968.
-
Kolb M, Vašáková M. Respir Res. 2019;20(1):57.
-
Wollin L, et al. J Scleroderma Relat Disord. 2019;4(3):212-218.
-
Distler JHW, et al. Nat Rev Rheumatol. 2019;15(12):705-730.
-
Shumar JN, et al. J Clin Med. 2021;10(11):2285.
-
Vacchi C, et al. J Clin Med. 2020;9(2):407.
-
Spagnolo P, et al. Ann Rheum Dis. 2021;80(2):143-150.
-
Castelino FV, Moua T. ACR Open Rheumatol. 2021;3(5):295-304.
-
Swigris JJ, et al. Eur Respir Rev. 2018;27(150):180075.
-
van Manen MJG, et al. Respir Med. 2017;132:226-231.
-
Arcana Rl, et al. J Pers Med. 2023;13(11):1589.
-
Khor YH et al. Eur Respir Rev. 2025;34(177):250046.
-
Lee H et al. Sci Rep. 2024;14(1):8857.
-
Cassone G et al. J Clin Med. 2020;9(4):1082.
-
Olson AL et al. Am J Respir Crit Care Med. 2011;183(3):372-378.
-
Hyldgaard C et al. Respiration. 2019;98(5):455-460.
-
Juge P-A et al. RMD Open. 2023;9(4):e003491.
-
Hyldgaard C et al. Respirology. 2017;22(3):494-500.
-
Cappelli S et al. Eur Respir Rev. 2015;24(137):411-419.
-
Distler O et al. Eur Respir J. 2020;55(5):1902026.
-
Distler O et al. Expert Rev Clin Immunol. 2019;15(10):1009-1017.
-
Tyndall AJ et al. Ann Rheum Dis. 2010;69(10):1809-1815.
-
Steen VD, Medsger TA. Ann Rheum Dis. 2007;66(7):940-944.
-
Roofeh D et al. Curr Opin Rheumatol. 2019;31(3):241-249.
-
Geerts S et al. Sarcoidosis Vasc Diffuse Lung Dis. 2017; 34: 326-335.
-
Kolb M et al., Eur Respir Rev. 2018;27(150):180071.
-
Strykowski R, Adegunsoye A. Immunol Allergy Clin North Am. 2023;43(2):209-228.
-
OFEV Prescribing Information. Boehringer Ingelheim International GmbH. May 2025.
-
OFEV Summary of Product Characteristics. Boehringer Ingelheim International GmbH. March 2025.
-
Koudstaal T, Wijsenbeek MS. Presse Med. 2023;52(3):104166.
-
Alsomali H et al. Pulm Ther. 2023;9:177–93.
-
Delameilleure A et al. ERJ Open Res. 2022;8:00030–2022.
-
Majewski S et al. Front Pharmacol. 2025;16:1586197.
-
Qiu Y et al. Ther Adv Respir Dis. 2024;18:1–12.
-
Romero Ortiz AD et al. BMJ Open Respir Res. 2024;11:e001687.
-
Corral M et al. BMC Pulm Med. 2020;20:188.
-
Santoleri F et al. J Pharm Pract. 2022;35:853–8.
-
Takehara K et al. Cells. 2022;11:143.
-
Zhao R et al. Pulm Pharmacol Ther. 2024;84:102287.
-
Galli JA et al. Respirology. 2017;22:1171–8.
-
Richeldi L et al. N Engl J Med. 2014;370:2071–82.
-
Flaherty KR et al. N Engl J Med. 2019;381:1718–27.
-
King TE Jr et al. N Engl J Med. 2014;370:2083–92.
-
Vancheri C et al. Eur Respir J. 2010;35(3):496–504.
-
Zheng Q et al. ERJ Open Res. 2022;800591–2021.
-
Chen X et al. Front Pharm. 2021;12:754851.
-
Cen Z et al. Ann Med. 2024;56:2406439.
-
Kwon BS et al. Respir Res. 2021;22:282.
AT/RESP/0426/PC-AT-105383
